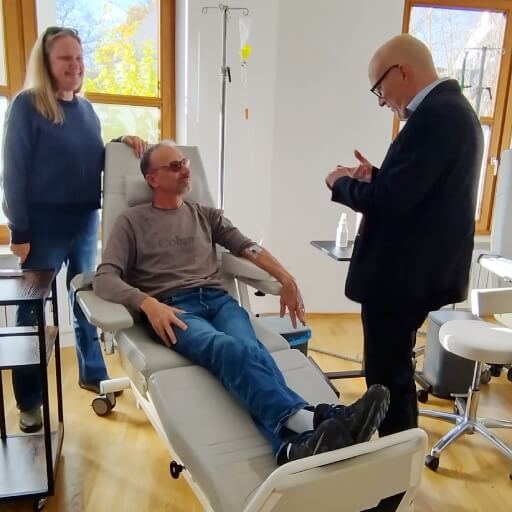
يُشَكّل سرطان البروستاتا (PCa) تهديداً صحياً كبيراً بين الرجال في منتصف العُمر وكبار السن حول العالم. تتوقع تقديرات جمعية السرطان الأمريكية تشخيص نحو 313.780 حالة إصابة جديدة بسرطان البروستاتا في عام 2025، كما يُتوَقّع وفاة عدد كبير من الرجال يصل إلى حوالي 35.770 رجُلاً بسبب هذا المرض. وهذا يعني تشخيص إصابة رجل واحد بسرطان البروستاتا (CaP) كل دقيقتين [1].
يَبلُغ معدل تطور المرض الحالي 120.2 حالة لكل 100.000 رجل سنوياً بناءً على بيانات 2018 - 2022، مع إصابة ما يقرُب من 1 من كل 8 رجال (12.9٪) بسرطان البروستاتا (PC) خلال حياتهم [2]. ما يُثير القلق حقاً هو أنه بعد انخفاض عدد حالات المرحلة المتقدمة بين عامي 2007 و 2014، تغيرت الأمور. فمنذ عام 2014، بدأت معدلات سرطان البروستاتا في الارتفاع بنسبة 3٪ كل عام. كما تزداد تشخيصات المرحلة المتقدمة حتى بوتيرة أسرع – بنسبة تتراوح بين 4.6٪ و 4.8٪ سنوياً. وعند النظر إلى معدلات البقاء على قيد الحياة، فإن الرجال الذين يعانون من سرطان البروستاتا في مرحلة متقدمة لديهم فرصة بنسبة 38٪ فقط للبقاء على قيد الحياة لمدة خمس سنوات. قارن هذا بالمرض الموضعي حيث تكون النسبة 100٪ تقريباً [2].
استُخدِمت برامج النظائر العلاجية باللوتيتيوم-177-PSMA، والأكتينيوم-225-PSMA، والراديوم-223 بنجاح في علاج السرطان المتقدم. هذه أدوية حديثة، والتي عمل العلماء خلال تطويرها على تصحيح أوجه القصور المرتبطة بالنظائر المُستخدَمة سابقاً. ومع بروز نظير الأكتينيوم-225 كبديل واعد لنظيري اللوتيتيوم-177 والراديوم-223، من الضروري فهم فوائد كل علاج للسرطان، ومؤشرات استخدامه، وآثاره الجانبية المُحتملة.
ما يواجهه المرضى عندما يُصبح سرطان البروستاتا متقدماً
إن تطور سرطان البروستاتا النقيلي المقاوم للإخصاء (mCRPC) يعني أن خيارات العلاج أصبحت أكثر محدودية. ويَجري العمل على إنتاج جيل جديد من مثبطات مستقبلات الأندروجين والعوامل الكيميائية العلاجية. إلا أن مُقاومة خلايا الورم للأدوية الحالية تستدعي إيجاد أساليب علاجية جديدة.
تعتبر خلايا سرطان البروستاتا النقيلي المقاوم للإخصاء mCRPC غير متجانسة بطبيعتها، مما يُشكل تحديات فريدة. فحوالي 80-90٪ من المرضى يصابون بنقائل عظمية في الغالب، بينما يعاني آخرون من تَورّط واسع للعقد اللمفاوية، أو مرض حشوي – وكلٌّ منها يتطلب اعتبارات علاجية مختلفة. أحدثت العلاجات المُوجّهة بالنويدات المُشعّة تغييراً جذرياً في مشهد علاج السرطان عندما تم إدخالها إلى الممارسة السريرية. فهي تُقدم أملاً جديداً للمرضى الذين جَرّبوا بالفعل جميع خيارات العلاج التقليدية.
يشمل العبء المالي المُترتب على الإصابة بسرطان البروستاتا المتقدم التكاليف الطبية المباشرة وغير المباشرة (مثل فقدان القدرة على العمل). تشير بيانات جمعية السرطان الأمريكية إلى أن النفقات التي يتحملها المرضى لعلاجات السرطان تُقدَّر بمبلغ ضخم يصل في المتوسط إلى 21.1 مليار دولار سنوياً.
إن الاختلافات الجغرافية في الوصول إلى علاجات السرطان المتقدمة كبيرة. فالدول ذات مستويات التطور العالية لديها برامج لـ الطب النووي، إلا أن العديد من الرجال يضطرون للسفر إلى الخارج للخضوع لبرامج النظائر المشعة باستخدام الأكتينيوم-225-PSMA وغيره من النويدات المشعة. وهذا يُبرز الحاجة إلى التوسع المستمر في مراكز العلاج المتخصصة التي تُنتج النويدات المشعّة.
العلاج بالروابط المشعة في سرطان البروستاتا النقيلي
يُعد العلاج بالروابط المشعة Radioligand therapy أحد الأساليب المبتكرة لعلاج سرطان البروستاتا والذي يُسهم في تعزيز فعالية العلاج. حيث يجمع بين دقة الاستهداف الجزيئي وقوة الإشعاع المضادة للورم، مما يؤدي إلى نتائج أفضل ومعدلات بقاء على قيد الحياة أعلى للمرضى. في السنوات الأخيرة، أصبح هذا العلاج الجديد بالروابط المشعة خطوةً مهمة في إدارة سرطان البروستاتا النقيلي، حتى في الحالات التي تكون فيها العلاجات التقليدية غالباً محدودة الفعالية في السيطرة على تطور المرض.
يعمل العلاج بالروابط المشعة (RLT) عن طريق توصيل الإشعاع مباشرةً إلى موقع السرطان عن طريق ربط النظائر المشعة بجزيء يرتبط بمستضد مُحدد مرتبط بالورم يُطلق عليه الرابط Ligand. وينتُج عن ذلك تركيز عالٍ من الجسيمات المشعة مباشرةً في الورم. ويُساعد هذا النهج في الحفاظ على الأنسجة السليمة ويُسبب آثار جانبية أقل.
غالباً ما تُعبر خلايا سرطان البروستاتا عن مستضد غشاء البروستاتا النوعي (PSMA). ويُعتبر هذا الجزيء أداة مثالية لـ العلاج الموجه بالروابط المشعة. يسمح التركيز العالي بوصول المزيد من جزيئات الروابط إلى الورم وتوصيل جزيئات مشعة إضافية، مما يُحسن من فعالية العلاج. تُعد إجراءات اللوتيتيوم-177 PSMA والأكتينيوم-225 PSMA أمثلة سريرية على كيفية عمل RLT عن طريق حماية الأنسجة السليمة واستهداف الخلايا السرطانية والقضاء عليها.
يسمح العلاج بالروابط المشعة RLT بتحديد الجرعة بدقة والقدرة على تكرار العلاج لعدة دورات، مما يجعله أحد الخيارات العلاجية الرئيسية لسرطان البروستاتا النقيلي. ففي كل عام، يتم اكتشاف المزيد من جزيئات الروابط المشعة التي توفر استهدافاً أفضل وأكثر تنوعاً للسرطان.
إحداها هو العلاج بالروابط المشعة FAPI، الذي يستخدم بروتين تنشيط الأرومة الليفية الموجود في البيئة المجهرية للورم. وقد يكون هذا مفيداً ليس فقط للورم الأولي ولكن أيضاً لتدمير النقائل ومنع تكوينها. كما أنه يُمثل إمكانية جديدة لعلاج أورام البروستاتا التي لا تُعبّر عن PSMA.
يمكن دمج هذا الإجراء ضمن خطة علاجية للمرضى المصابين بسرطان البروستاتا النقيلي. فهو يجمع بين التصوير التشخيصي والعلاج الدقيق، مما يجعله علاجاً شخصياً للغاية. يمكن تعديلة وفقاً للملف الجزيئي الفريد لكل ورم، مما يعكس مبادئ طب الأورام الحديث.
مؤشرات استخدام اللوتيتيوم-177 والأكتينيوم-225 والراديوم-223 في سرطان البروستاتا
هناك عاملين رئيسيين يُسببان اختلافات في عمل برامج النظائر التي تستخدم جُسيمات مُشعّة مختلفة:
- الخصائص الفيزيائية للجُسيم المُشع في تركيبه هي نوع الإشعاع، ونصف قطر الإشعاع للأنسجة المحيطة، وعُمر النصف بعد الإنتاج
- خصائص الجزيء الحامل للجُسيمات المُشعّة تتضمن الموثوقية وكفاءة الاستهداف
| النويدات المشعة | مؤشرات الاستخدام | مبدأ العمل العلاجي |
|---|---|---|
| نظير اللوتيتيوم-177-PSMA يُنتج إشعاع بيتا (إلكترونات عالية الطاقة)، عُمر النصف – 6.5 أيام | سرطان البروستاتا النقيلي المقاوم للإخصاء P-Ca، وخاصةً مع نقائل العظام | كان نظير اللوتيتيوم-177 أول نويدة مشعة تحصل على موافقة إدارة الغذاء والدواء الأمريكية FDA للاستخدام في علاج سرطان البروستاتا. الجزيء الحامل في هذا الدواء هو PSMA، وهو مستضد غشائي خاص بالبروستاتا. تُمثل مستقبلات PSMA على سطح الخلايا السرطانية هدفاً فريداً ترتبط به النويدات المشعة العلاجية بعد إعطائها وريدياً. بنصف عُمره الذي يبلغ 6.5 أيام، فإن إشعاع اللوتيتيوم-177-PSMA لا يمتد إلى أكثر من 100-200 خلية غير سرطانية مُحيطة. |
| نظير الأكتينيوم-225-PSMA العلاج المُوجَّه بأشعة ألفا (نوى الهيليوم)، عُمر النصف – 10 أيام | سرطان البروستاتا النقيلي المقاوم للإخصاء P-Ca، وخاصةً مع نقائل العظام | لعلاج سرطان البروستاتا النقيلي، يرتبط نظير الأكتينيوم-225 بنفس الجزيء الحامل الذي يرتبط به نظير اللوتيتيوم-177 – PSMA. تختلف آلية عمل الدواء نتيجة استبدال النظير: إذ يستمر تأثير الأكتينيوم-225 لمدة 4 أيام إضافية، ويقتصر نصف قطر عمله على 1-2 خلية مُحيطة فقط. ونتيجة لذلك، يكون العلاج بالأكتينيوم-225 فعالاً حتى في حالة عدم وجود استجابة مُرضِية لنظير اللوتيتيوم-177. |
| نظير اللوتيتيوم-177-DOTATAT يُنتج إشعاع بيتا (إلكترونات عالية الطاقة)، عُمر النصف – 6.5 أيام | سرطان البروستاتا العصبي الصماوي (NEPC) | في هذه الحالة، يرتبط النظير المشع اللوتيتيوم-177 بمادة حاملة مختلفة، وهي جزيء DOTATATE. يتمتع DOTATATE بألفة تركيبية لمستقبلات السوماتوستاتين، والتي تتواجد بكثرة على سطح الأورام العصبية الصماوية. بعد الحقن الوريدي، يتراكم نظير اللوتيتيوم-177-DOTATAT في الأورام العصبية الصماوية للبروستاتا ويدمرها، مُحافِظاً على الوظائف الطبيعية للمثانة والأمعاء. |
| نظير الراديوم-223 يُنتج إشعاع ألفا الطبيعي (نوى الهيليوم)، علاج ألفا غير الموجَّه، عُمر النصف: 11.5 يوماً | سرطان البروستاتا النقيلي المقاوم للإخصاء PCa، وخاصةً مع نقائل العظام | من حيث التركيب، يُشبه الراديوم عنصر الكالسيوم، وهو العنصر البنيوي الرئيسي لأنسجة العظام. وبفضل هذا، فإنه يندمج في عملية الاستقلاب الطبيعي للعظام ويُشعِّع بشكل محدد الخلايا السرطانية المتكاثرة بنشاط في نقائل العظام. يؤثر إشعاع ألفا للراديوم-223 على ما بين 2-10 خلايا محيطة، أما الدواء، الذي لا تمتصه العظام، فيتم إفرازه سريعاً عبر الأمعاء (نظراً لعُمر النصف البالغ 11.5 يوماً). وتشير بيانات الدراسات السريرية إلى أنه عند استخدام هذا الدواء، تتلقى الخلايا السرطانية إشعاعاً أكثر بـ 8-9 مرات مقارنةً بالأنسجة السليمة. |
وافقت إدارة الغذاء والدواء الأمريكية (FDA) على إنتاج نظائر اللوتيتيوم-177-PSMA-617 لعلاج سرطان البروستاتا النقيلي المقاوم للإخصاء في صيف عام 2021. كما تُجرَى تجارب سريرية على العلاج باللوتيتيوم في المراحل المبكرة من سرطان البروستاتا (P-Ca). حتى الآن، مؤشرات استخدام العلاج باللوتيتيوم Lutetium-177-PSMA-617 هي كما يلي:
- سرطان البروستاتا النقيلي مع تطور نقائل في العظام، والعقد اللمفاوية، والرئتين
- عدم الاستجابة للعلاج الهرموني والعلاج الكيميائي
- وجود موانع للعلاج الهرموني والعلاج الكيميائي
- وجود عدد كافٍ من مستقبلات PSMA على سطح الخلية بناءً على فحص PSMA-PET/CT الأولي باستخدام Gallium-68
تعديل آخر لنظير اللوتيتيوم-177، وهو اللوتيتيوم-177-DOTATAT، وهو مخصص للمرضى الذين يعانون من سرطان البروستاتا العصبي الصماوي النادر (NEPC). يتم وصف أربع دورات من علاج السرطان باستخدام اللوتيتيوم-177-DOTATAT، بفاصل زمني 8 أسابيع بين الإجراءات في حالة:
- وجود موانع للجراحة أو العلاج الكيميائي
- عدم فعالية الجراحة السابقة أو العلاج الكيميائي السابق
- الفشل في التحديد الدقيق لخصائص الخلايا السرطانية، ووجود النقائل وعددها
يُعدّ إعطاء نظير الأكتينيوم-225-PSMA بديلاً آخر لعلاج السرطان بالنويدات المشعة. يمكن إعطاؤه عند فشل نظير اللوتيتيوم-177-PSMA. وبالتالي، يُتاح للرجال خياران، ويتيح علاج السرطان بالأكتينيوم-225 PSMA تطوير علاجات للسرطان أكثر تخصيصاً. قد يقوم أطباء الأورام بإعطاء الأكتينيوم-225 بالاشتراك مع العلاج باللوتيتيوم-177، كبديل مباشر، أو للمرضى المؤهلين، قبل العلاج الكيميائي. انتقال الطاقة الخطي العالي ومرونة الإعطاء يجعل نظير الأكتينيوم-225 جزءاً قيّماً من العلاج الموجه لسرطان البروستاتا المتقدم.
تُعدّ جُسيمات ألفا عالية الطاقة لنظير الأكتينيوم-225 نقلة نوعية في علاج السرطان. وقد أظهرت دراسة WARMTH Act (يمكن الاطلاع عليها في مجلة The Lancet Oncology, 2024) نتائج استثنائية لدى 488 مريض في 7 مستشفيات دولية، بمتوسط بقاء على قيد الحياة إجمالي قدره 15.5 شهراً [3]. وهذا يُرسّخ مكانة نظير الأكتينيوم-225 كعلاج رائد.
تمتلك جسيمات ألفا عالية الطاقة لنظير الأكتينيوم-225 مزايا علاجية فريدة: عُمر النصف للنظير يبلغ 10 أيام ونفاذية للأنسجة بمقدار 1-2 قطر خلوي. وبالتالي، يقوم الأكتينيوم-225 بتوصيل الإشعاع إلى الخلايا السرطانية المُعبرة عن PSMA مع الحفاظ على الأنسجة السليمة [4].
إنتاج نظير الراديوم-223 يهدف بشكل رئيسي إلى علاج النقائل العظمية في سرطان البروستاتا المتقدم. تُنشّط نقائل العظام التي تحتوي على خلايا سرطان البروستاتا الخلايا المُكوِّنة للعظم، وهي خلايا غير سرطانية ذات نشاط أيضي مُكثف مسؤولة عن بناء العظام. تُرَاكِم الخلايا المُكوِّنة للعظم أيونات الكالسيوم بنشاط، نظراً للتشابه البنيوي، الأمر الذي يُمكّن الراديوم-223 المُشع من التغلغل في النقائل. هذا يجعل الراديوم-223 الدواء الأمثل لـ:
- سرطان البروستاتا النقيلي المؤكد مع تطور نقائل عظمية مُكوِّنة للعظم
- غياب (أو وجود عدد قليل) من النقائل في الأعضاء الداخلية (العقد الليمفاوية، والكبد، والرئتين)
بالإضافة إلى علاج السرطان، تُستخدم النويدات المشعة أيضاً بنشاط في تشخيص سرطان البروستاتا. على سبيل المثال، يشمل الفحص التشخيصي باستخدام النويدات المشعة عادةً التصوير باستخدام Gallium-68-DOTATATE (لسرطان البروستاتا العصبي الصماوي) و PSMA PET/CT باستخدام Gallium-68 (لسرطان البروستاتا).
| العلاج | المؤشّرات الأولية | نمط المرض | العلاجات السابقة | التعبير عن PSMA | المزايا الرئيسية |
|---|---|---|---|---|---|
| اللوتيتيوم-177-PSMA | mCRPC مع وجود خلايا سرطانية إيجابية لـ PSMA | خلايا سرطانية عظمية + نقائل الأنسجة الرخوة | بعد علاج ARPI، وبعد العلاج الكيميائي | SUVmax مرتفعة >20 | معتمد من إدارة الغذاء والدواء الأمريكية (FDA)، متوفر على نطاق واسع |
| الأكتينيوم-225-PSMA | mCRPC، وتقدم المرض بعد العلاج بـ Lu177 | تطور المرض عالي الحجم | عدة خطوط علاجية سابقة | SUVmax متوسطة إلى عالية | علاج بإشعاع ألفا المُوجّه المتفوق، علاج إنقاذي |
| نظير الراديوم-223 | mCRPC مع نقائل العظام | الآفات العظمية المُكوِّنة للعظم فقط | بعد ARPI | غير مطلوب | مخصص للعظام، تخفيف الألم |
| اللوتيتيوم-177-DOTATAT | سرطان البروستاتا العصبي الصمّاوي | NEPC مع وجود مستقبلات السوماتوستاتين | عند وجود موانع للجراحة/العلاج الكيميائي | غير قابل للتطبيق | استهداف محدد لـ NEPC |
ما مدى فعالية الأدوية في علاج سرطان البروستاتا النقيلي؟
تعتمد فعالية العلاج باستخدام الأدوية المشعة على عدة عوامل:
- خصائص الخلايا السرطانية
- استراتيجية العلاج السابقة والاستجابة للعلاج
- برنامج النظير المُشعّ والعامل الدوائي المشعّ
- مدة برنامج النظير المشعّ ومدى دمجه مع الخيارات العلاجية القياسية
اللوتيتيوم-177-PSMA لعلاج سرطان البروستاتا النقيلي
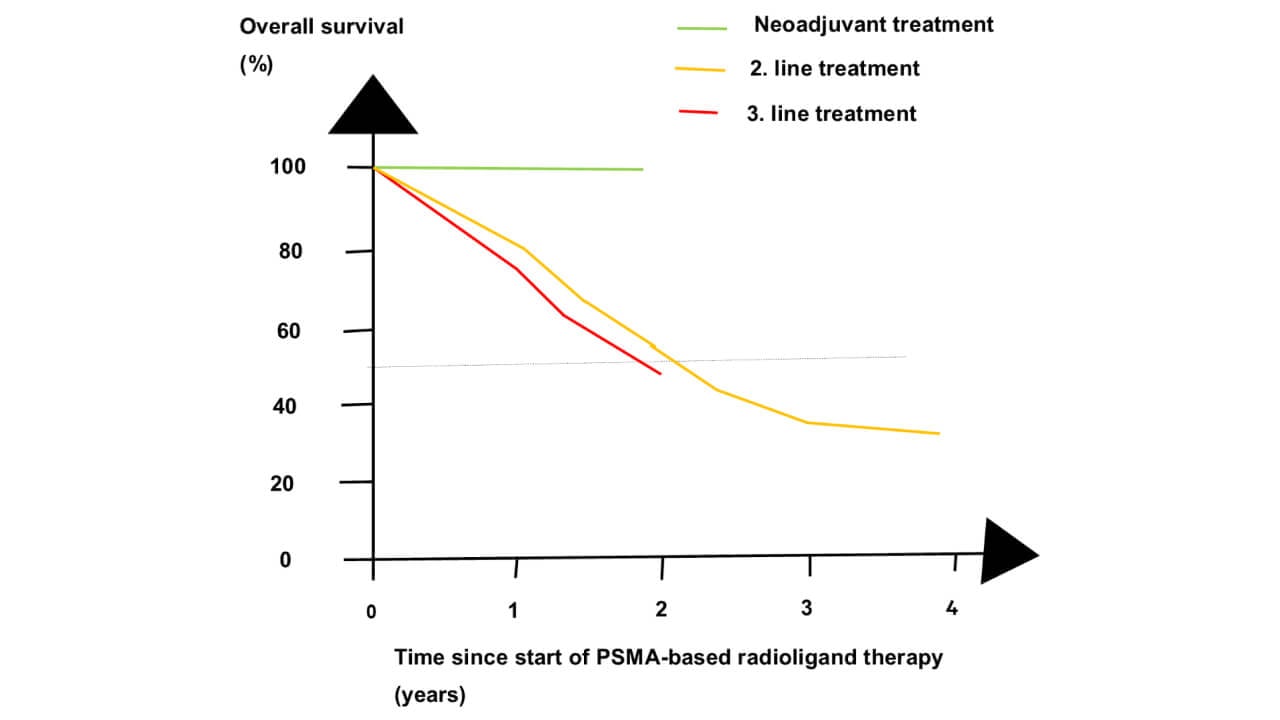
استكشفت عدة تجارب سريرية الفعالية السريرية لإنتاج وإعطاء نظائر اللوتيتيوم-177، والأكتينيوم-225، والراديوم-223. ووفقاً لنتائج تجربة VISION السريرية، حصل إنتاج اللوتيتيوم-177-PSMA على موافقة إدارة الغذاء والدواء الأمريكية (FDA) وتصنيفه كـ "علاجاً ثورياً" لسرطان البروستاتا النقيلي المقاوم للهرمونات في عام 2021. بعد دورة علاجية واحدة أو عدة دورات بالعلاج باللوتيتيوم-177-PSMA، ارتفع معدل البقاء على قيد الحياة لمدة 5 سنوات لمرضى سرطان البروستاتا النقيلي إلى 30٪. كما انخفض خطر تكرار المرض؛ حيث استمرت الهدأة من المرض لدى 30-40٪ من المرضى لمدة عامين.
البروفيسور دريزل، الخبير الرائد في الطب النووي، يكشف عن قوة العلاج باللوتيتيوم-177
الأكتينيوم-225-PSMA لعلاج سرطان البروستاتا النقيلي
التجارب على الأكتينيوم-225 PSMA، باعتباره دواءً أكثر ابتكاراً، لا تزال جارية، إلا أن النتائج التي تم الحصول عليها حتى الآن تُظهر انخفاضاً بنسبة 50-80٪ في عدد النقائل وانخفاضاً بنسبة 90٪ في مستويات مستضد البروستاتا النوعي لدى 82٪ من الرجال. وقد أظهرت دراسة حديثة واسعة النطاق، تُعرف باسم WARMTH Act (العلاج بالرابط المشع باستخدام الأكتينيوم-225-PSMA لسرطان البروستاتا النقيلي المقاوم للإخصاء، mCRPC)، نتائج مُشجعة لدى الرجال المصابين بسرطان البروستاتا المتقدم.
أثبتت المراجعات المنهجية الحديثة أن إعطاء جسيمات ألفا عالية الطاقة من الأكتينيوم-225 يُعد خياراً علاجياً متفوقاً. وقد أجرى تحليل تلوي شامل دراسة على 1.155 مريضاً عبر دراسات دولية متعددة. وأفادت الدراسة بمعدلات استجابة مُجمعة لـ PSA50 بلغت 65٪ لعلاج الأكتينيوم-225. وهذه النسبة أعلى بكثير من المعدلات المُعتادة لعلاج اللوتيتيوم-177-PSMA، والتي تتراوح بين 49٪ و 59٪ [4].
أظهرت دراسة WARMTH Act متعددة المراكز نتائج استثنائية لدى المرضى الذين تلقوا علاجاً مكثفاً مسبقاً. من بين 488 رجلاً عُولِجوا في سبعة مراكز في أستراليا، والهند، وألمانيا، وجنوب إفريقيا، بلغ متوسطالبقاء على قيد الحياة 15.5 شهراً. وبلغ متوسط البقاء على قيد الحياة دون تطور المرض 7.9 شهراً [3]. والجدير بالذكر أن المرضى الذين لم يخضعوا للعلاج الكيميائي سابقاً حققوا متوسط بقاء إجمالي بلغ 24.2 شهراً، بينما حقق أولئك الذين لم يتعرضوا لنظير اللوتيتيوم-177 سابقاً 18.8 شهراً.
تنبُع الفعالية الفائقة للأكتينيوم-225 من خصائصه الفريدة لـ العلاج المُوجَّه بأشعة ألفا. بفضل قِيَم انتقال الطاقة الخطية التي تفوق إشعاع بيتا بـ 500 مرة واقتصار اختراقه للأنسجة على 50-80 ميكرومتر فقط، يوفر الأكتينيوم-225 إشعاعاً دقيقاً وعالي الطاقة. وهذا يؤدي إلى حدوث كسور غير قابلة للإصلاح في شريط DNA مزدوج السلسلة بغض النظر عن مرحلة دورة الخلية السرطانية، أو إنتاج الطاقة، أو حالة الأكسجين.

نظير الأكتينيوم -225 مقابل نظير اللوتيتيوم -177 لسرطان البروستاتا النقيلي
تستمر الأبحاث حول التفوق السريري ومؤشرات استخدام الأكتينيوم-225 / اللوتيتيوم-177. يرتبط الأكتينيوم-225 PSMA بمستقبلات خلايا الورم بشكل أقوى، ويمتاز بعُمر نصفي أطول بنسبة 60٪ من عُمر نصف اللوتيتيوم-177. وبالتالي، يضمن إنتاج تأثير أطول أمداً في نقاشات الفعالية السريرية لـ اللوتيتيوم-177 مقابل الأكتينيوم-225. كما يتم حماية الأنسجة السليمة، إذ يقتصر نطاق نصف قطر تأثيره على خلية أو خليتين فقط (مقارنةً بـ 100-200 خلية غير سرطانية للوتيتيوم-177). لذلك، في نقاشات المقارنة بين اللوتيتيوم-177 والأكتينيوم-225، يبدو أن الأكتينيوم-225 متفوقاً.
في الأوراق الطبية المنشورة على الإنترنت وعلى مستوى العالم، نجد أدلة قوية على فعالية الأكتينيوم-225: معدلات استجابة أعلى لمستويات مستضد البروستاتا النوعي في الأكتينيوم-225 (65-82٪) مقارنةً باللوتيتيوم-177 (40-60٪). وتتضح هذه الميزة بشكل أكبر لدى المرضى الذين يعانون من مرض متقدم [5].
يتجلى تفوق جسيمات ألفا عالية الطاقة للأكتينيوم-225 بشكل خاص في الحالات المقاومة للعلاج. فبينما تنخفض معدلات استجابة اللوتيتيوم-177 بشكل ملحوظ بعد العلاجات السابقة، يحافظ الأكتينيوم-225 على فعاليته القوية حتى لدى المرضى الذين تقدمت حالتهم بعد تلقي علاجات سابقة متعددة، بما في ذلك اللوتيتيوم-177 نفسه، مما يُشير إلى آلية مختلفة للتغلب على مقاومة خلايا السرطان.
الراديوم-223 لعلاج سرطان البروستاتا النقيلي
تمت دراسة عملية إنتاج وإعطاء الراديوم-223 في تجربة ALSYMPCA السريرية التي شملت 921 رجلاً. ووفقاً لنتائج التجربة، زاد الدواء متوسط البقاء على قيد الحياة الإجمالي بمقدار 3.6 شهراً، وخفض خطر الوفاة بنسبة 30٪، كما قلل بشكلٍ كبير من خطر حدوث كسور مرضية في العمود الفقري. في الوقت نفسه، خفّض الدواء بشكل موثوق متلازمة الألم الناتجة عن نقائل العظام، مما سمح بتصنيفه كطريقة فعالة لعلاج الأعراض. وقد حصل الدواء على موافقة إدارة الغذاء والدواء الأمريكية (FDA) منذ عام 2013.
الراديوم-223 مقابل اللوتيتيوم-177 لسرطان البروستاتا النقيلي
يُعد إنتاج كل من الراديوم-223 واللوتيتيوم-177 طريقتان معتمدتان من إدارة الغذاء والدواء الأمريكية FDA، وهما مُدرجتان ضمن المبادئ التوجيهية القياسية لعلاج سرطان البروستاتا النقيلي. ومع ذلك، يتميز الراديوم-223 بعُمر نصف أطول من اللوتيتيوم-177، مما يضمن تأثيراً علاجياً أطول. بالإضافة إلى ذلك، يعمل الراديوم-223 ضمن نطاق 10 خلايا فقط كحد أقصى على عكس اللوتيتيوم-177. تساعد مثل هذه الخصائص على حماية الأنسجة السليمة من التأيُّن.
ومع ذلك، تُشير بعض الدراسات إلى ارتفاع معدَّلات الوفيات بين المرضى الذين عُولِجوا سابقاً بالرايديوم قبل خضوعهم للعلاج باللوتيتيوم مقارنةً بالأشخاص الذين لم يخضعوا للعلاج بالراديوم. علاوةً على ذلك، تمَّ الإبلاغ عن تطور المرض بوتيرة أعلى قليلاً لدى المرضى الذين عُولِجوا بالراديوم-223 مقارنةً باللوتيتيوم-177. وبالتالي، في حالة المُفاضلة أو الجدل بين إنتاج وإعطاء الرايديوم مقابل اللوتيتيوم، فقد ترجح كفّة الأخير استناداً إلى عددٍ من المؤشرات السريرية الحاسمة.
بشكلٍ عام، يُؤدي العلاج باستخدام اللوتيتيوم-177 والأكتينيوم-225 والراديوم-223 إلى تحسُّن كبير في حالة معظم المرضى الذين يعانون من سرطان البروستاتا في مراحله المتقدمة. يُنصح بهذا العلاج بشكلٍ واضح للرجال الذين يعانون من خلايا سرطانية مقاومة للهرمونات مع نقائل في العظام، والعقد اللمفاوية، والكبد، والرئتين. إمكانية الاختيار بين نظائر مُشعّة مختلفة من حيث الإنتاج وطريقة الإعطاء تتيح للأطباء تخصيص العلاج بما يتناسب مع حالة كل مريض وتحقيق نتائج علاجية ممتازة.
| الخصائص | اللوتيتيوم-177 | الأكتينيوم-225 | الراديوم-223 |
|---|---|---|---|
| الاستجابة للعلاج | انخفاض حجم الورم بنسبة 30-80٪ | انخفاض عدد النقائل بنسبة 50-80٪ | 30-٪50 |
| مستويات PSA | انخفاض بنسبة 70٪ | انخفاض مستويات PSA بنسبة 90٪ | انخفاض بنسبة 20-30٪ |
| معدل تكرار المرض | انخفاض بنسبة تصل إلى 40٪ | انخفاض في تَقدُم المرض بنسبة 40-60٪* | انخفاض في تَقدُم المرض بنسبة 15-30٪ |
| معدلات البقاء على قيد الحياة بشكل عام | زيادة بنسبة تصل إلى 30٪ | زيادة بنسبة 30٪* | زيادة طفيفة في البقاء علي قيد الحياة |
| متوسط البقاء على قيد الحياة الإجمالي | 15.3 شهراً (تجربة VISION) | 15.5 شهراً (دراسة WARMTH Act) | 14.9 شهراً (تجربة ALSYMPCA) |
| البقاء على قيد الحياة بدون تطور المرض | 8.7 شهراً | 7.9 شهراً | 2.8 شهراً |
| الوقت حتى الأحداث الهيكلية | 11.5 شهراً | لم يتم تحديده بعد | 15.6 شهراً |
| معدل استجابة الألم | 40-٪50 | 60-٪70 | 70-٪80 |
*قد تختلف البيانات اعتماداً على عوامل المريض الفردية.
تسلسل العلاج واتخاذ القرارات السريرية في سرطان البروستاتا النقيلي
خوارزمية العلاج المُثلى لسرطان البروستاتا المتقدم
يتطلب استخدام النظائر المُشعّة العلاجية تخطيطاً دقيقاً لتسلسل العلاج. تدعم الأدلة الحالية اتباع نهج شخصي يعتمد على تقييم شامل لخصائص المرض، والعلاجات السابقة، وحالة أداء المريض.
بالنسبة لمرضى mCRPC الذين لم يسبق علاجهم ويُظهِرون تعبيراً عالياً عن مستوى PSMA مع وجود نقائل مختلطة في العظام والأنسجة الرخوة، يبرُز العلاج بالأكتينيوم-225-PSMA كخيار علاجي مُفضل من الخط الأول. ويعود ذلك إلى معدلات الاستجابة العالية لمستضد البروستاتا النوعي وإمكانية تحقيق هدأة مستقرة. العلاج الموجه بأشعة ألفا يوفر علاج فعّال للنقائل مع الحفاظ على الأنسجة الطبيعية.
يُعدّ المرضى المصابون بنقائل عظمية مُكوِّنة للعظم مرشحين للعلاج بالراديوم-223 من حيث الإنتاج والإعطاء (كعلاج الخط الأول). كما أنه ممكن أيضاً في حالة الحد الأدنى من تورط الأنسجة الرخوة. يُعتبر هذا العلاج ذا قيمة خاصة للمرضى الذين يُعطون الأولوية لجودة حياتهم نظراً لخواصه التلاصقية مع العظام وفوائده المُثبتة في تخفيف الأعراض.
يُعدّ اللوتيتيوم-177-PSMA خياراً علاجياً مهماً للمرضى الذين يعانون من عبء مرضي متوسط والذين قد يستفيدون من التوافر واسع النطاق وملف السلامة المُثبت للعلاج بإشعاع بيتا. يستمر دور برامج النظائر المُشعّة هذه كعلاج جسري أو في البروتوكولات المتسلسلة في التطور.
استراتيجيات العلاج المتسلسل
تَطَوُّر المرض بعد العلاج باللوتيتيوم-177 يمثل نقطة قرار حاسمة حيث أظهر الأكتينيوم-225-PSMA فعالية استثنائية كعلاج إنقاذي. معدلات الاستجابة البالغة 50-60٪ لدى المرضى المقاومين للعلاج باللوتيتيوم-177 تشير إلى أن العلاج الموجه بأشعة ألفا يمكن أن يتغلب على آليات المقاومة التي تحد من فعالية العلاج المنبعث من بيتا [6].
تخضع الأساليب العلاجية المُركبة التي تستخدم العلاج المتسلسل باستخدام العلاج الموجه بأشعة ألفا وبرامج النظائر المُشعّة بيتا لدراسات مكثفة. وتشير النتائج الأولية للتجارب المُركبة إلى فعالية مُحَسّنة مع ملف سُمّية قابل للإدارة، مما قد يمثل مستقبل العلاج بالنظائر المُشعّة الشخصي المُخصص.
خيارات العلاج بعد العلاج بالراديوم-223 تشمل كِلا العلاجان الموجهان ضد PSMA، مع اختيار العلاج بناءً على مستويات التعبير عن PSMA وانتشار المرض. قد تؤثر فترة تعافي نخاع العظم بعد العلاج بالراديوم-223 على التوقيت الأمثل للعلاجات اللاحقة.
ما هي ردود الفعل والآثار الجانبية التي قد تحدث أثناء علاج سرطان البروستاتا النقيلي؟
اليوم، في الممارسة السريرية للمراكز والأقسام المتخصصة في الطب النووي، لا تُستخدم إلا النظائر المُشعّة ذات مستوى الأمان الأمثل والحد الأدنى من الآثار الجانبية. تُوصف برامج النظائر المُشعّة للمرضى الضعفاء المصابين بمراحل متقدمة من السرطان، ولذلك، يولي الأطباء اهتماماً خاصاً ليس فقط لفعالية العلاج بل أيضاً لقابلية المرضى لتحمّله.
تشمل الآثار الجانبية الأكثر شيوعاً لبرامج النظائر ما يلي:
- جفاف الفم – 87٪ من المرضى
- الغثيان – 50٪ من المرضى
- التعب – 50٪ من المرضى
- فقر الدم – 13٪ من المرضى
- نقص الصفائح الدموية – 13٪ من المرضى
- نقص اللمفاويات – 37٪ من المرضى
يُعد جفاف الفم أو xerostomia أكثر الآثار الجانبية شيوعاً، إلى جانب التعب. كما يتميز كل من اللوتيتيوم-177 والأكتينيوم-225 بانخفاض سُميتهما على نخاع العظم، أي أنهما لا يؤثران على النخاع الشوكي عند علاج النقائل في العمود الفقري والعظام الأخرى (التوطين الأكثر شيوعاً للنقائل في سرطان البروستاتا). معظم الآثار الجانبية مؤقتة وتزول من تلقاء نفسها في غضون أيام أو أسابيع قليلة بعد انتهاء دورة العلاج. يُسبب العلاج بالأكتينيوم، والعلاج باللوتيتيوم، والعلاج بالراديوم آثاراً جانبية أقل بكثير على المدى القصير والطويل مقارنةً بالعلاجات التقليدية نظراً لكفاءة الاستهداف العالية. وإذا لزم الأمر، قد يصف الأطباء علاجاً للأعراض، مثل الأدوية المضادة للغثيان أو أدوية لتحسين الحالة العامة للمريض.
مقارنة ملفات السلامة والأمان في علاج سرطان البروستاتا النقيلي
لقد قدمت تحليلات السلامة الحديثة رؤى تفصيلية حول ملفات التحمل لبرامج النظائر المختلفة، مما يسمح باختيار العلاج بشكل أكثر استنارة بناءً على عوامل الخطر الخاصة بكل مريض.
بالرغم من قدراته القوية في العلاج الموجه بأشعة ألفا، يُظهر الأكتينيوم-225-PSMA ملف أمان ممتاز. فقد أفادت دراسة WARMTH Act بحدوث أحداث سلبية من الدرجة 3-4 لدى 17٪ فقط من المرضى، مع كَون فقر الدم (11٪) ونقص الصفائح الدموية (6٪) أكثر أنواع السُمية الشديدة شيوعاً [3]. والجدير بالذكر أنه لوحظ جفاف الفم الشديد لدى أقل من 5٪ من المرضى، وهي نسبة أقل بكثير من المعدلات التاريخية للعلاجات الأخرى المستهدِفة لـ PSMA.
يبدو أن دقة العلاج الموجه بأشعة ألفا تُقلل من الضرر الجانبي للأنسجة السليمة. وتبقى وظائف الكلى، التي تُعدّ مصدر قلق بالغ في العلاجات المستهدِفة لـ PSMA، مستقرة لدى معظم المرضى الذين يتلقون الأكتينيوم-225، مع تسجيل سُمّية كلوية من الدرجة 3-4 في أقل من 3٪ من الحالات.
| فئة الآثار الجانبية | اللوتيتيوم-177-PSMA | الأكتينيوم-225-PSMA | الراديوم-223 |
|---|---|---|---|
| الدموية (من الدرجة 3-4) | |||
| فقر الدم | ٪20-15 | ٪11 | ٪15-10 |
| نقص الصفائح الدموية | ٪15-10 | ٪6 | ٪10-5 |
| نقص الخلايا المتعادلة | ٪12-8 | ٪4 | ٪5-2 |
| غير الدموية (من أي درجة) | |||
| جفاف الفم (Xerostomia) | ٪90-80 | ٪80-70 | ٪20-10 |
| غثيان | ٪60-50 | ٪50-40 | ٪40-30 |
| إسهال | ٪30-20 | ٪20-15 | ٪50-40 |
| سُمية خاصة بالأعضاء | |||
| السُمية الكلوية (من الدرجة 3-4) | ٪8-5 | ٪3-2 | <٪1 |
| جفاف الفم الشديد | ٪15-10 | <٪5 | <٪1 |
| تثبيط نخاع العظم | مُعتدل | خفيف | مُعتدل |
*المصادر: تجارب سريرية متعددة وتحليلات السلامة، 2021-2025
استراتيجيات الحد من المخاطر وإدارتها
أصبحت الإدارة الاستباقية للآثار الجانبية أكثر تطوراً، مع وضع بروتوكولات متخصصة يتم تطويرها لكل برنامج علاجي بالنظائر المشعة. بالنسبة لجفاف الفم، وهو أكثر الآثار الجانبية شيوعاً المرتبطة بعلاج PSMA، تشمل التدابير الوقائية حماية الغدد اللعابية قبل العلاج باستخدام الكمادات الباردة وتناول أدوية محفزة لإفراز اللعاب بعد العلاج.
تخضع المراقبة الدموية لبروتوكولات معيارية دقيقة مع تأجيل العلاج أو تعديل الجرعات اعتماداً على تعافي تعداد الدم. يسمح ملف السُميّة النخاعية المنخفضة للعلاج بالأكتينيوم-225 بقدر أكبر من المرونة في جدولة الجلسات العلاجية مع إمكانية تحسين جودة حياة المرضى أثناء العلاج.
تم إنشاء برامج مراقبة ومتابعة طويلة الأمد لرصد الآثار المتأخرة، ولا سيما الأورام الخبيثة الثانوية واختلال وظائف الأعضاء. وتُظهِر بيانات المتابعة الحالية، الممتدة حتى خمس سنوات بعد العلاج، إلى عدم وجود زيادة في معدلات الإصابة بسرطان ثانوي مقارنةً بالعلاجات القياسية.
قصص نجاح من مرضى سرطان البروستاتا
تُجسّد قصة جون بيكر إصراراً قوياً ومُثابرة في البحث عن أفضل حل لمشكلته. عانى جون من سرطان البروستاتا لمدة 5 سنوات: بدأ العلاج الإشعاعي الموجه والعلاج الحراري فوراً بعد التشخيص. ولكن التأثير كان غير مُلهم رغم ذلك. لم ينجح العلاج كما كان يأمل.
في ذلك الوقت تقريباً، اكتشف جون أن السرطان انتشر خارج البروستاتا. كان هذا خبراً سيئاً. واجه جون وزوجته تحدياً كبيراً. كان بإمكانهم انتظار موافقة التأمين، والتي عادةً ما تستغرق وقتاً طويلاً. أو استكشاف خيارات علاجية أخرى. وكان ذلك بالضبط عندما عثروا على Booking Health واللوتيتيوم-177.
اتصل جون وزوجته بمتخصصي Booking Health من أجل بدء العلاج في أقرب وقتٍ ممكن. "كل شيء سار كالساعة"، يقول السيد بيكر، مستذكراً تجربته في الخضوع للعلاج باللوتيتيوم-177 في ألمانيا. تم التخطيط لكل خطوة من خطوات العملية بشكلٍ جيد وتم التواصل بوضوح. "لم أشعر أبداً بالقلق بشأن المكان الذي أذهب إليه"، قال جون بيكر. لم يُسبب العلاج في حد ذاته أي شعور بعدم الارتياح أو آثار جانبية. "الشيء الوحيد الذي كان مُتعباً هو رحلة الطائرة"، قال السيد بيكر ضاحكاً. لم يقتصر الأمر على عدم وجود آثار ضارة على عكس العلاج الكيميائي الكلاسيكي أو غيره من طرق البروتوكول، بل إن فعالية العلاج باللوتيتيوم-177 أقنعت جون بأن قرار المجيء إلى ألمانيا لتلقي العلاج كان يستحق العناء. بعد جلسة واحدة من العلاج، أظهر الفحص عدم وجود آفات نقيلية في العظام. وفوق ذلك، انخفضت مستويات PSA بشكل ملحوظ. "أود أن أوصي به لأي شخص يعاني من أي مشكلة متعلقة بالسرطان، وليس فقط سرطان البروستاتا. إنه واضح ومباشر وبسيط للغاية"، هكذا اختتم السيد بيكر حديثه.
"انخفض مستوى PSA إلى الصفر": مريض أمريكي يشارك رحلته في علاج السرطان في ألمانيا
استعادة أمل جديد مع العلاج بالأكتينيوم-225 PSMA لسرطان البروستاتا
كان كريستوفر لامبي يكافح سرطان البروستاتا لعدة سنوات. لقد جرب العديد من الطرق القياسية بما في ذلك الهرمونات والعلاج الكيميائي. ومع ذلك، استمر المرض في التَقدُم مع القليل من الأمل المتبقي عندما تم اكتشاف النقائل أثناء فحص آخر مُخطط له. وبدون الكثير من الحماس، قرر السيد لامبي البحث عن رأي بديل في الخارج. هذه هي الطريقة التي تعرف بها على شركة Booking Health.
بعد التواصل الأولي والتحليل الشامل للحالة، تمت التوصية للسيد لامبي ببدء العلاج بالأكتينيوم-PSM A225. "كنت مُتشكك للغاية في البداية. لم أكن أعرف شيئاً عن هذا الأكتينيوم: ما هو وكيف سأتعامل معه". عندما وصل المريض، تم اصطحابه من المطار برفقة مترجم شخصي. "لقد سارت الأمور بسلاسة تامة: كان لدي سائق خاص، ومترجم، ومدير، كان على اتصال معي حرفياً طوال الوقت"، قال كريستوفر لامبي. وبعد إجراء الاختبارات الطبية واستشارة شخصية أخرى، بدأ السيد لامبي علاجه في اليوم التالي مباشرةً. بعد خضوعه لبروتوكول العلاج القياسي، كان كريستوفر لامبي خائفاً من الآثار الضارة الشديدة التي كان لها تأثير كبير على حياته وعمله. لقد فوجئ بسرور بعدم ظهور أي آثار جانبية بعد العلاج بالأكتينيوم-PSMA 225. "كان الأمر لا يُصدق – لا نزيف، ولا تقيؤ، ولا تساقط للشعر. كان الإجراء سهلاً للتنفيذ". وكان السيد لامبي متفاجئاً أكثر عندما رأى فحصه التالي أثناء المتابعة، والذي أظهر أن ما يقرب من 90٪ من النقائل قد اختفت بعد جلسة واحدة فقط. "كنت على وشك أن أفقد الأمل بعد الكثير من النضال. والآن يمكنني العودة إلى العمل. لم أحلم بذلك مرة أخرى". يشعر كريستوفر لامبي بالامتنان لأنه اختار ذات مرة استخدام Booking Health لتنظيم علاجه في ألمانيا. "أفضل استثمار قمت به حتى الآن"، قال السيد لامبي ضاحكاً.
أين يمكن الحصول على علاج سرطان البروستاتا باستخدام اللوتيتيوم-177 والأكتينيوم-225 والراديوم-223؟
تُقدّم مراكز الطب النووي والأقسام المتخصصة في المستشفيات الجامعية الكبرى العلاج بالنظائر المشعة. هذه قائمة ببعض أفضل المؤسسات الطبية التي يمكن لأي شخص الوصول إليها من أي بلد في العالم:
- مستشفى جامعة ريختس دير إيزار ميونخ، قسم الطب النووي. يرأس القسم البروفيسور الدكتور في الطب فولفجانج فيبر، المتخصص في علاج السرطان بالنويدات المشعة. أعد البروفيسور أكثر من 250 مقالاً للمجلات العلمية الرائدة، بما في ذلك مجلة Journal of Clinical Oncology.
- مستشفى جامعة لودفيغ ماكسيميليان ميونخ، قسم الطب النووي. يرأس القسم البروفيسور الدكتور في الطب ماتياس برندل، وهو خبيرٌ مؤهلٌ تأهيلاً عالياً يتمتع بخبرة واسعة في علاج الأورام بالإشعاع. لدى البروفيسور برندل أكثر من 200 منشور علمي ويشارك بانتظام في المؤتمرات الوطنية والدولية المُخصصة للتشخيص والعلاج بالنظائر المشعة.
- مستشفى هيليوس برلين-بوخ، قسم الطب النووي. يرأس القسم البروفيسور الدكتور في الطب ستيفان دريزل، الذي كرّس أكثر من 22 عاماً لممارسة الطب النووي. يتخصص في العلاج باللوتيتيوم-177 PSMA لسرطان البروستاتا المتقدم، والعلاج باللوتيتيوم-177-DOTATOC للأورام العصبية الصماوية. يُساهم البروفيسور دريزل بنشاط في البحث العلمي من خلال العديد من المنشورات ويشارك بانتظام في المؤتمرات الطبية الدولية التي تُركز على التطورات في الطب النووي.
- مستشفى كارل غوستاف كاروس الجامعي دريسدن، قسم الطب النووي. رئيس القسم البروفيسور الدكتور في الطب يورج كوتزركي. يعمل البروفيسور في مجال أساليب التشخيص والعلاج بالنظائر المشعة لأكثر من ثلاثين عاماً وهو عضو مجلس إدارة الجمعية الألمانية للطب النووي (DGN).
- مستشفى جامعة إرلنغن، قسم الطب النووي. رئيس القسم البروفيسور الدكتور في الطب تورستن كوفرت. يعمل البروفيسور في معاهد الطب النووي والمستشفيات الجامعية منذ ما يقرب من 30 عاماً؛ وهو الآن يتخصص في علاج سرطان البروستاتا ونقائله.
تحليل فعالية تكلفة علاج سرطان البروستاتا
يمتد التأثير الاقتصادي للعلاجات بالنظائر المشعة ليشمل أكثر من مجرد تكاليف العلاج الأولية. أظهرت التحليلات الاقتصادية الشاملة أن هذه العلاجات المتقدمة تتمتع بملفات إيجابية فعالة من حيث التكلفة عند مقارنتها بالعلاجات التقليدية.
صحيح أن العلاج باللوتيتيوم-177-PSMA له تكاليف أولية مرتفعة، إلا أنه أظهر نسب فعالة من حيث التكلفة عند الأخذ بعين الاعتبار سنوات العُمر المُعدَّلة بحسب جودة الحياة المكتسَبة (QALYs). أما العلاج بالأكتينيوم-225 فهو أكثر تكلفة لكل دورة علاجية. لكن عند النظر في خيارات العلاج المختلفة، لا ينبغي أن تُخيفك تكاليف العلاج بالروابط المشعة، إذ يُعد من أكثر الخيارات فعاليةً عندما يتعلق الأمر بالنتائج السريرية، ومدة العلاج، وفترة الإقامة في المستشفى، مما يساهم في تقليل التكاليف والمضاعفات المرتبطة.
| علاج سرطان البروستاتا | متوسط تكلفة العلاج في ألمانيا | متوسط تكلفة العلاج في الولايات المتحدة الأمريكية |
|---|---|---|
| علاج سرطان البروستاتا مع النقائل باستخدام اللوتيتيوم-177-PSMA | 17.000 € - 28.000 € | تبدأ من 55.000 $ لكل دورة |
| علاج سرطان البروستاتا مع النقائل باستخدام الأكتينيوم-225-PSMA | 15.000 € - 29.000 € | تبدأ من 60.000 $ لكل دورة |
| علاج سرطان البروستاتا مع نقائل العظام باستخدام الراديوم-223 | 21.700 € - 23.700 € | تبدأ من 32.000 $ لكل دورة |
| العلاج باللوتيتيوم-177-DOTATATE لسرطان البروستاتا العصبي الصماوي (NEPC) | 14.000 € - 28.000 € | غير متوفر على نطاق واسع |
علاج سرطان البروستاتا بالنويدات المشعة في أفضل المستشفيات الرائدة في العالم مع Booking Health
غالباً لا يستطيع مرضى سرطان البروستاتا الخضوع للعلاج باللوتيتيوم-177 أو الأكتينيوم-225 أو الراديوم-223 في بلدانهم الأصلية لأن إنتاج المواد المشعة وتوفير حماية عالية من الإشعاع عمليات صعبة من الناحية التقنية. لهذا السبب يبحثون عن فرص مناسبة في المستشفيات الأجنبية. Booking Health هي وكيل سياحة طبية تعمل على تنظيم العلاج بالنويدات المشعة في المراكز الطبية النووية الرائدة لمرضى سرطان البروستاتا الذين يعانون من أعراض من 75 دولة لأكثر من 12 عاماً.
وبصفتها شركة مرموقة، تُقدم Booking Health خطط شخصية لعلاج المرحلة الرابعة من سرطان البروستاتا مع حجز مباشر للمستشفى ودعم كامل في كل مرحلة، بدءاً من العمليات التنظيمية وحتى المساعدة أثناء العلاج. نحن نقدم:
- تقييم وتحليل التقارير الطبية
- تطوير برنامج الرعاية الطبية
- اختيار موقع العلاج المناسب
- إعداد الوثائق الطبية وإرسالها إلى المستشفى المناسب
- الاستشارات التحضيرية مع الأطباء لتطوير برامج الرعاية الطبية
- نصائح الخبراء أثناء الإقامة في المستشفى
- رعاية المتابعة بعد عودة المريض إلى بلده الأصلي بعد إكمال برنامج الرعاية الطبية
- الاهتمام بالإجراءات الرسمية كجزء من التحضير لبرنامج الرعاية الطبية
- تنسيق وتنظيم إقامة المريض في بلد أجنبي
- المساعدة في الحصول على التأشيرات وتذاكر السفر
- مُنسق شخصي ومترجم فوري مع دعم على مدار الساعة 24/7
- عدم وجود رسوم خفية في فواتيرك
الصحة جانب لا يُقدر بثمن في حياتنا. ينبغي تفويض إدارة شيء هش للغاية ولكنه ثمين فقط إلى خبراء يتمتعون بخبرة مُثبتة وسمعة طيبة. تُعد Booking Health شريك جدير بالثقة يساعدك في الحصول على صحة أقوى وجودة حياة أفضل. اتصل بمستشارنا الطبي لمعرفة المزيد عن إمكانيات العلاج الشخصي باستخدام طرق مبتكرة لسرطان البروستاتا النقيلي مع أفضل المتخصصين الرائدين في هذا المجال.
علاج السرطان المتقدم: قصص نجاح المرضى مع Booking Health
الأسئلة الشائعة حول سرطان البروستاتا النقيلي
تواصل مع أخصائي طبياللوتيتيوم-177 والأكتينيوم-225 هما علاجان يستهدفان PSMA باستخدام أنواع مختلفة من الإشعاع (بيتا، وألفا، على التوالي). أما الراديوم-223 فهو أكثر فعالية في علاج نقائل العظام. ويتمتع نظير اللوتيتيوم-177 بنطاق إشعاعي أكبر، بينما يدوم الأكتينيوم-225 لفترة أطول وله نطاق إشعاعي أقصر، مما يُساعد في الحفاظ على الأنسجة السليمة.
يُوصى عادةً بهذه العلاجات للمرضى المصابين بسرطان البروستاتا النقيلي المقاوم للإخصاء (mCRPC)، والذين لم يستجيبوا بشكلٍ جيد للعلاجات الأخرى مثل العلاج الهرموني والعلاج الكيميائي. يعتمد الاختيار المُحدد على كمية وموقع النقائل، والعلاجات السابقة، والحالة الصحية العامة.
تشمل الآثار الجانبية الشائعة التعب، والغثيان، وانخفاض مؤقت في عدد خلايا الدم. وقد يحدث جفاف الفم مع جميع العلاجات التي تستهدف PSMA. كما قد يُسبب الراديوم-223 الإسهال في بعض الأحيان. وتُعتبر هذه الآثار الجانبية قابلة للإدارة بشكلٍ عام وأقل شدة من الآثار الجانبية للعلاج الكيميائي التقليدي.
أظهرت التجارب السريرية نتائج واعدة. فعلى سبيل المثال، أظهر العلاج باللوتيتيوم-177-PSMA معدلات استجابة لـ PSA تتراوح بين 40-60٪ ومعدلات استجابة موضوعية تتراوح بين 40-50٪ في بعض الدراسات. وأظهر الأكتينيوم-225-PSMA معدلات استجابة أعلى حتى في التجارب المبكرة. وثَبُتَ أن الراديوم-223 يُحسّن معدل البقاء على قيد الحياة الإجمالي لدى المرضى الذين يعانون من نقائل عظمية.
في كثير من الحالات، يكون إجراء واحد كافياً للحصول على نتيجة سريرية. كما أن الإجراءات المتكررة مُمكنة: 4-6 للوتيتيوم-177-PSMA، و 2-4 للأكتينوم-225-PSMA، و 6 للراديوم-223.
حالياً، نظير الأكتينيوم-225 غير متوفر بنفس درجة توفر نظير اللوتيتيوم-177 (Lu-177). ومُستحضرات Lu-177 يمكن الوصول إليها في العديد من الدول وفي مرافق رعاية صحية مختلفة.
كقاعدة عامة، يُعتبر العلاج بـ Ac-225 أكثر تكلفة بسبب ارتفاع تكاليف إنتاج نظير الأكتينيوم-225. ومع ذلك من باب المُفارقة، قد تكون التكلفة الإجمالية للعلاج أقل باستخدام الأكتينيوم-225 لأنه عادةً ما يتطلب عدد جلسات علاجية أقل.
نعم، وفقاً لاستنتاجات الدراسات الأولية. قد يُحسن العلاج المُركّب باستخدام نظير Ac-225 ونظير Lu-177 من فعالية البروتوكولات العلاجية.
تُظهِر أورام البروستاتا النقيلية الخبيثة نفسها عادةً على شكل آلام في العظام، وتعب، وفقدان الوزن. وفي اختبارات الدم، يتم الكشف عن ارتفاع مستويات PSA على خلفية العلاج المستمر.
تبلغ تكلفة العلاج باللوتيتيوم-177 PSMA حوالي 17.000 € - 28.000 € لكل دورة، بينما تبلغ تكلفة العلاج بالأكتينيوم-225 PSMA – حوالي 18.000 € - 29.000 €. يمكنك التحقق من السعر في مستشفى مُحدد على موقع Booking Health.
يُستخدم العلاج بالأكتينيوم‑225‑PSMA في حالة الرجال المصابين بسرطان البروستاتا النقيلي المقاوم للإخصاء – خاصةً عندما لا يعمل العلاج باللوتيتيوم-177-PSMA كما هو متوقع. حالياً، يمكن اعتبار العلاج بالأكتينيوم خيار الخط الأول.
يُلاحظ مُقدمو الرعاية والمرضى انخفاضاً كبيراً في نشاط السرطان، حيث تنخفض مستويات PSA بنسبة تصل إلى 90٪ (في ما يصل إلى 82٪ من الحالات). ويُعد تقييم مستوى PSMA قبل العلاج أمراً ضرورياً للتنبؤ بالاستجابة.
يُقلل العلاج باستخدام الأكتينيوم-225 من تقدم وتكرار السرطان – حيث يوفر تحسُّناً بنسبة 40-60٪ مقارنةً بالبروتوكولات القياسية.
يتمتع المرضى الذين عولجوا باستخدام الأكتينيوم-225-PSMA بتحسُّن في معدل البقاء على قيد الحياة الإجمالي بحوالي 30٪ مقارنةً بالعلاجات القياسية.
مستشفى جامعة ريختس دير إيزار ميونخ، ومستشفى جامعة لودفيغ ماكسيميليان ميونخ، ومستشفى هيليوس برلين بوخ، ومستشفى جامعة إرلنغن – تعد هذه المستشفيات متخصصة في علاجات النويدات المشعة.
تُقدم ألمانيا رعاية من الطراز العالمي لسرطان البروستاتا المتقدم. فهنا يجمع الأطباء بين الأساليب العلاجية المبتكرة والقياسية في ظل بروتوكولات سريرية صارمة (بهدف تحقيق أقصى قدر من النتائج).
يهدف العلاج بالروابط المشعة Radiogland therapy إلى توصيل النظائر المشعة مباشرةً إلى الورم. ويستخدم جزيئات خاصة تستهدف البروتينات التي تُعبر عنها الأورام. وينتج عن ذلك التدمير الدقيق لخلايا سرطان البروستاتا النقيلي مع تقليل الضرر الذي يلحق بالأنسجة السليمة.
يعمل العلاج الموجه بالروابط المشعة على العثور على مستضدات مُحددة يتم التعبير عنها بواسطة الخلايا السرطانية. ويوصل العلاج موضعياً، مما يساهم في تقليل عبء الورم وتخفيف الأعراض، وقد يؤدي إلى إطالة البقاء على قيد الحياة.
تعتمد تكلفة العلاج بالروابط المشعة على النظير المُستخدم وعدد دورات العلاج التي يتم إجراؤها. كما يمكن أن تتأثر التكلفة أيضاً بالتشخيصات الإضافية ومدة الإقامة في المستشفى.
اختر العلاج في الخارج وستحصل بالتأكيد على أفضل النتائج!
المؤلفون:
تم تحرير المقال من قبل خبراء طبيين وأطباء معتمدين من مجلس الأطباء الدكتورة ناديجدا إيفانيسوفا و الدكتورة يانا دميتريشين. لعلاج الحالات المشار إليها في المقال، يجب استشارة الطبيب؛ المعلومات الواردة في المقالة ليست مخصصة للتطبيب الذاتي!
سياستنا التحريرية، التي توضح بالتفصيل التزامنا بالدقة والشفافية، متاحة هنا. انقر على هذا الرابط لمراجعة سياساتنا.
المصادر:
[1] ZERO Prostate Cancer. Facts & Statistics.
https://zerocancer.org/about-prostate-cancer/facts-statistics
[2] National Cancer Institute. SEER Cancer Stat Facts: Prostate Cancer.
https://seer.cancer.gov/statfacts/html/prost.html
[3] Actinium-225-PSMA radioligand therapy of metastatic castration-resistant prostate cancer (WARMTH Act): a multicentre, retrospective study. Sathekge, Mike M et al. The Lancet Oncology, Volume 25, Issue 2, 175 - 183.
https://www.thelancet.com/journals/lanonc/article/PIIS1470-2045(23)00638-1/abstract
[4] Ninatti G, et al. Time for action: actinium-225 PSMA-targeted alpha therapy for metastatic prostate cancer - a systematic review and meta-analysis. Theranostics. 2025;15:3386-3399. DOI: 10.7150/thno.106574. [DOI]
[5] Garo ML, et al. [225Ac]Ac-PSMA for the treatment of metastatic castration-resistant prostate cancer: A systematic review and meta-analysis. Eur J Clin Invest. 2025;55:e14358 DOI: 10.1111/eci.14358. [DOI]
[6] Benedikt Feuerecker, Robert Tauber, Karina Knorr et al. Activity and Adverse Events of Actinium-225-PSMA-617 in Advanced Metastatic Castration-resistant Prostate Cancer After Failure of Lutetium-177-PSMA, European Urology, Volume 79, Issue 3, 2021, Pages 343-350, ISSN 0302-2838, https://doi.org/10.1016/j.eururo.2020.11.013. [DOI]
[7] MDPI. Review on the Increasing Role for PSMA-Based Radioligand Therapy in Prostate Cancer.
https://www.mdpi.com/2072-6694/16/14/2520#
اقرأ:
دليل شامل للحصول على علاج سرطان البروستاتا
علاج المرحلة الرابعة من سرطان البروستاتا في ألمانيا: ما تحتاج إلى معرفته